高密度微载体生物反应器大规模培养
作者:艾贝泰 2024.09.24 点击566次
河南省预防型疫苗工程技术研究中心,河南省生物医药产业研究院与河南省生物医药工程技术研究中心等多个团队通力合作,在生物制品学杂志发表关于生物反应器大规模培养狂犬病病毒的成果,该研究为150 L生物反应器高密度微载体工艺放大提供了技术支持,为后期开发更大规模高密度微载体反应器工艺奠定基础。
狂犬病病毒(rabies virus, RABV)是致死率极高的病毒,分布于多种哺乳动物宿主,这些宿主与人类之间存在复杂的关系。目前,RABV引起的狂犬病每年造成约5.9万人死亡。迄今为止,狂犬病发病后几乎无治愈病例,主要通过提前接种疫苗来进行预防。我国每年人用狂犬病疫苗的消耗量约1600万人份。对于狂犬病疫苗的制备,RABV大规模扩增是关键技术,也是决定成本的重要因素之一。目前主要采用生物反应器(借助微载体)培养Vero细胞,扩增RABV,再纯化病毒等步骤制备狂犬病疫苗,具有成本较低、技术较易控制等优点,本研究在30 L生物反应器的基础上,尝试采用150 L生物反应器、高密度微载体培养Vero细胞,扩增RABV,以期为规模化培养RABV,制备狂犬病疫苗提供参考。
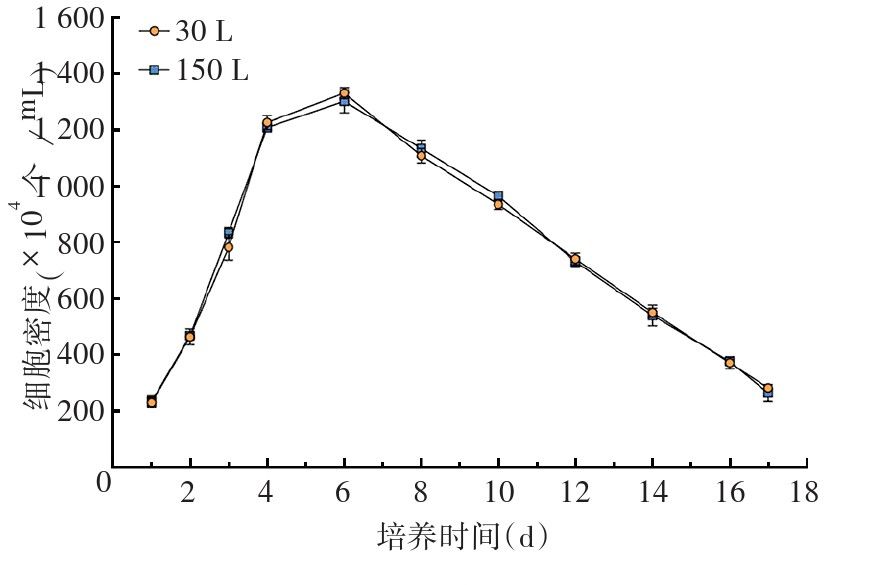
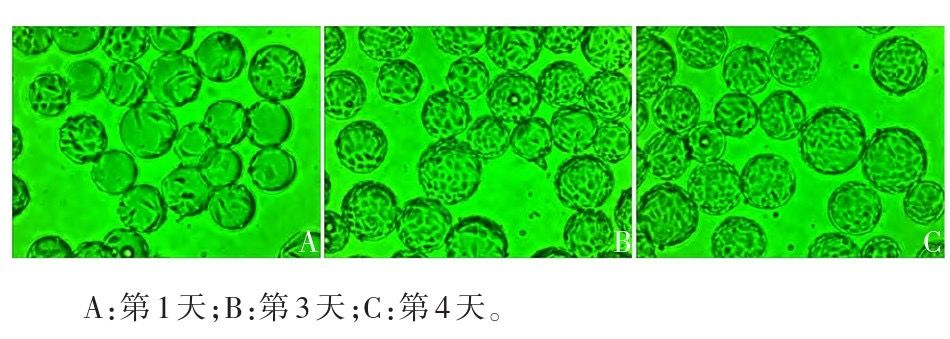
应用30 L和150 L生物反应器,以灌流方式培养Vero细胞和CTN-1V株RABV, Cytodex-1微载体浓度20 g/L,培养温度36~38℃,DO 20%~60%,pH 7.0~7.4,连续13 d收获病毒液,培养过程中取样检测细胞密度、病毒滴度,并对病毒收获液进行无菌和支原体检查及抗原、宿主细胞蛋白(host cell protein, HCP)、牛血清白蛋白(bovine serum albumin, BSA)、DNA残留量检测。结果30 L和150 L生物反应器的细胞培养密度均可达1.2×107个/mL以上,在培养过程中各时间点的细胞密度差异均无统计学意义(t=0.225~2.173, P=0.096~0.833)。2种规模生物反应器病毒收获液均在感染后6 d达最高病毒滴度(8.5 lgLD50/mL),且差异无统计学意义(t=1.000, P=0.374)。2种规模生物反应器病毒收获液的抗原、HCP、BSA和DNA残留量基本一致。可用150 L生物反应器大规模培养RABV,病毒收获液符合《中国药典》三部(2020版)相关标准。 摇瓶工艺 摇瓶中细胞培养至第4天时,呈致密单层,接种RABV毒种。 生物反应器工艺 细胞培养过程中2种规模生物反应器的细胞密度变化趋势相似。细胞培养至第4天,密度达12.0×106个/m L以上,30 L生物反应器的细胞密度(12.3×106个/m L)高于150 L生物反应器(12.1×106个/m L),但二者差异无统计学意义(t=1.138, P=0.319)。接毒后细胞持续生长一段时间,2种规模生物反应器细胞密度均在第6天达最高,分别为13.3×106和13.0×106个/m L。随着病毒培养时间的延长,细胞密度呈下降趋势。2种规模生物反应器在培养过程中各时间点的细胞密度差异均无统计学意义(t=0.225~2.173, P=0.096~0.833)。细胞密度变化曲线见图1;接种细胞后,细胞贴附在微载体表面,形态饱满,无游离细胞,第4天呈致密单层,见图2;接种病毒后,细胞逐渐发生病变,从微载体上脱落,死亡,第13天大部分细胞已脱落,见图3。
图1
图2
图3
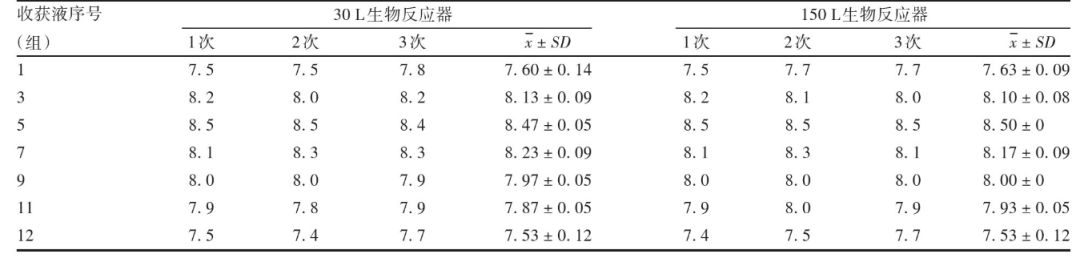
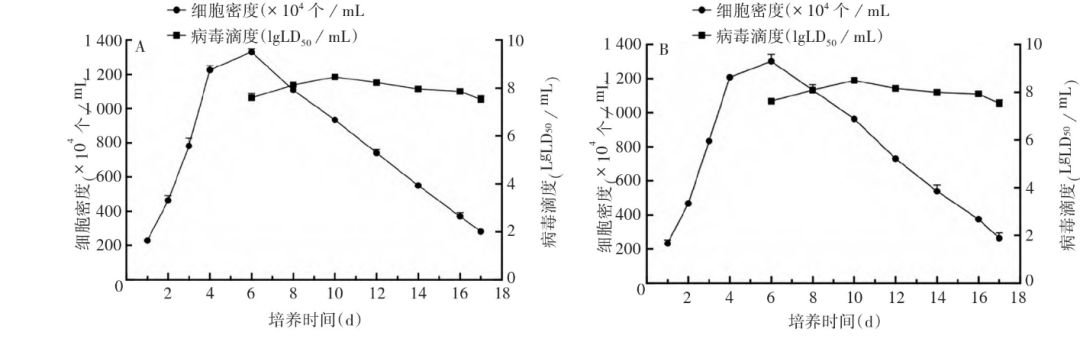
病毒收获液检定病毒滴度变化 30和150 L生物反应器中细胞感染2 d后收获的第1组病毒液滴度平均值分别为(7.60±0.14)和(7.63±0.09)lg LD50/m L;感染4 d后,2种规模生物反应器的细胞密度均下降、收获液病毒滴度均增加,均在感染后6 d达最高病毒滴度,且差异无统计学意义(t=1.000, P=0.374)。随后病毒滴度缓慢下降,培养结束时,2种规模生物反应器的收获液病毒滴度均为(7.53±0.12)lg LD50/m L。见表1和图4。表明从30 L放大至150 L的工艺可获得高滴度的病毒收获液。
表1
图4
结果摇瓶培养目前主要作为细胞培养扩增步骤,直接应用于规模化生产越来越少。单个摇瓶产能较小,规模化生产需至少数十个摇瓶同步进行,导致人工操作复杂且强度大,存在一定的暴露操作风险。摇瓶培养技术不再是规模化生产的发展方向。 应用生物反应器培养Vero细胞是疫苗制备的关键技术,是重要的发展方向之一。且生物反应器易操控,适合规模化放大,应用反应器微载体悬浮培养Vero细胞具有明显优势。生物反应器培养可获得更高的收益率,生物反应器的控制系统可以完成更多工作,可监测和控制的参数数量基于生物反应器中的传感器和控制元件数量,可以更好的进行培养工艺条件的筛选,优化。工艺简单、操作灵活,有良好的适用性;培养工艺容易放大,可为生物体生长和增殖提供均质的环境;产品质量稳定,非常适合工业化生产;管路布置较为简单,能提供较好的无菌条件,细胞生长过程中不易污染。该研究在30 L生物反应器规模实验的基础上,实现了在150 L生物反应器进行微载体浓度20 g/L的Vero细胞培养,并接种RABV,细胞病变过程正常且可控,病毒收获液滴度最高可达8.5 lg LD50/m L, 30和150 L生物反应器培养的终末代细胞各项检测均符合《中国药典》三部(2020版)要求,为后期开发更大规模高密度微载体生物反应器工艺奠定基础。 | 产品分类
重点推荐产品
|
 |